「アビガンが有望」と浮かれ、欧米中の速さに後れを取る
製薬業界の喫緊の課題は新型コロナウイルス特効薬の開発に尽きる。既に激烈な開発競争がグローバル規模で勃発している。
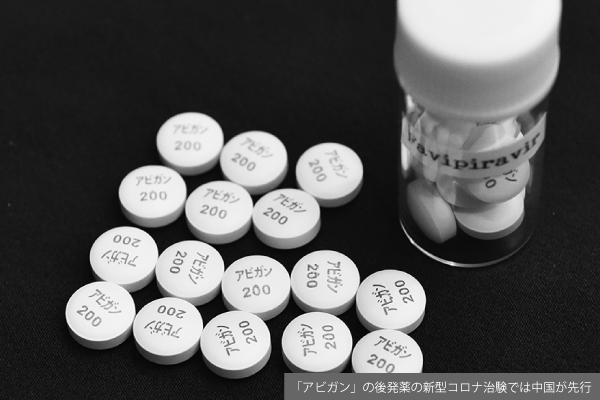
日本勢では富士フイルム富山化学のインフルエンザ治療薬「アビガン」が特効薬候補として最注目を集めている。
3月末には日本で富士フイルムが新型感染症向けに、人に薬を投与して有効性・安全性を調べる臨床試験(治験)3相の開始を発表した。
ただ、中国では既に治験に入っている。中国政府も3月17日に治験で有効な結果が出たと発表、診療指針にも採用する意向を見せている。
正確に言うと、中国の治験で使ったのは現地企業の浙江海正薬業のアビガン後発品。富士フイルムとのライセンス契約は既に契約期間終了だからだ。アビガンの物質特許も切れているから、この中国製後発品が中国で承認販売されても富士フイルムには一銭も入らない。
皮肉にも、本家より中国がアビガンの開発で一歩先を走っているのだ。
欧米メーカーも抜け目ない。未承認の治験薬「レムデシビル」を擁す米ギリアドがその筆頭だ。当初狙ったエボラ出血熱治療薬向けの治験は失敗に終わっていたが、新型ウイルスで再び脚光を浴びている。
米国立衛生研究所(NIH)、中国の大学、ギリアド等が主導する7つの治験が進行中。中国やギリアド主導試験の結果は4月、5月と立て続けに出てくる見込みだ。
しかも、企業治験は未承認薬なのに1相、2相を飛ばし、いきなりの3相。成功すれば承認となる。日本も国立国際医療研究センターがアビガン等の有望薬を後回しにして、この薬の治験にまず取り掛かる。レムデシビルが最有力とみているためだ。強調すべきは、NIH主導の国際共同治験に日本はあくまで参加する形で、日本が主導ではない事だ。
米中堅リジェネロンやスイスのロシュも既存薬を使い治験に入った。
これまで挙げた薬はみな治験や市販後調査で有効性や副作用等のデータが相当程度蓄積されている。種探しからの新薬開発なら承認までに優に10年かかるが、こうした既存薬の転用なら期間が大幅短縮出来る。新型ウイルスとの時間との闘いを考えれば、この道が最適ともいえる。
海外勢の開発速度は驚異的
もちろん新型ウイルス治療薬の一からの開発を目指す動きもある。
米バイオベンチャーのヴァル・バイオテクノロジーは新型コロナウイルス向けに特定した2つの抗体を中国企業に導出。米バイオ企業のアルナイラムと提携し、核酸医薬品も開発中だ。
武田薬品工業も3月初旬に回復した新型ウイルスの患者から採取した血漿を材料に作る免疫グロブリン製剤の開発を表明した。日本勢にしてはまれな素早い動きだが、治験開始時期は未確定。塩野義製薬等の意思表明はあるが具体性に欠ける。ここでも日本勢の動きは総じて鈍い。
感染防止効果ではさらに期待の高い予防用ワクチンの開発はどうか。
米バイオ企業のモデルナは3月16日に米国で治験を開始した。一からの開発でこの速さは驚異的だ。メッセンジャーRNA(mRNA)という遺伝子情報を使ったワクチンの高度な技術がその秘密だ。鶏卵等を使ってウイルス自体を培養する旧来のワクチンなら「製造するのに半年程度かかる」(大阪大学の森下竜一教授)。それに対し中国の、新型コロナウイルスの遺伝子情報公開から2カ月程度で前臨床を終え治験入りするのは半端ではない。
欧米勢の競争の激烈さを物語る事件も起きた。ドイツのバイオ企業キュアバクが買収されるという憶測記事が3月に入って出たのだ。ドイツの政府高官や著名大株主の反対やら、会社が正式に買収の事実を否定する等大騒ぎになった。
実は3月初旬、トランプ大統領が米国の製薬大手やバイオ企業等の首脳を呼び付けた。特効薬開発に発破をかける政治ショーだが、このドイツ企業も招かれ、憶測記事の伏線になった。6月の治験入りを狙うこのドイツ企業のmRNAワクチンが有望視されている証拠でもある。
mRNA陣営では米製薬大手のファイザーや中国製薬企業と協業するドイツの新興企業ビオンテックも4月中の治験入りを狙う。
日本勢ではバイオ企業アンジェスが孤軍奮闘する。生みの親の大阪大学の森下教授とタッグを組み、新型コロナウイルスのDNAワクチンの開発を3月5日に発表した。
DNAは遺伝子の本体。体をつくるたんぱく質産出の設計図の役割を果たす。このDNAをもとに転写されて出来るのがRNA。DNAワクチンはmRNAワクチンといわば親戚関係だ。製造期間が旧来のワクチンに比べ短縮できる優位性も同じ。3月26日には実際に実験用ワクチン製造をすませ動物試験段階に入った。日本企業では異例の速さだ。
ただ、それでも治験入りまでは「早くて半年はかかる」(森下教授)から、モデルナ等mRNA陣営を必死に追い掛ける構図だ。
3月末には米製薬大手ジョンソン&ジョンソンが9月までのワクチン治験入り、米国の市販前緊急許可法のもと、21年初の供給開始、10億回分以上の生産体制構築をぶち上げた。
欧米勢では仏サノフィ、英グラクソスミスクライン等多くの大手も参戦。3月に治験に入ったカンシノバイオロジクス等中国勢の動きも早い。
これに対し「製薬大手にも協力を求めてオール日本で臨みたい」(森下教授)の言葉がむなしく響くように日本の製薬大手の反応は乏しい。
官民とも基盤に実力差
流行が早く終われば、治験入りしても途中中断、大金を失うリスクが感染症治療薬の開発には付きまとう。事実、過去の重症急性呼吸器症候群(SARS)等では、承認されたワクチン等は出来ていない。
ただ、リスクは全世界共通。それでも海外勢が積極的なのはトランプ大統領の圧力もあるが、リスクにかける企業風土の彼我の違いが大きい。
国内の特効薬開発への政府支援も大きく違う。ポンと3000億円超を投じる米国に対し、日本は現状、300億円台の寒々しさ。民の背中を押す官の力も日本は弱いのだ。
従来とは桁違いの迅速な開発を可能にするmRNAワクチン等の、さらにそのベースになるのは遺伝子関連の技術だ。ここでも欧米勢に比べて、日本は大きく遅れる。
何よりそれを雄弁に物語るのは、遺伝子治療薬の開発の日米の違い。日本は昨年やっと先述したアンジェスが日本発第1号の承認薬を世に送り出したばかり。2億円超という世界最高の販売価格の付いた承認薬「ゾルゲンスマ」に続く開発が目白押しの欧米には、遠く及ぶべくもない。
要するに、リスクを後押しする官の力も弱ければ、そもそもリスクを担えるだけの技術を持つ企業群、産業基盤が薄いのが、今の日本の姿だ。
これが今回の新型コロナウイルス特効薬の開発でも表れている。ワクチンの場合でも新薬の承認・実用化までにはどう急いでも1年以上はかかる。まだ開発序盤で勝敗の即断は早いかもしれないが、新型コロナの特効薬開発競争でも日本勢が先陣を走る姿は想像が出来そうにない。




LEAVE A REPLY